
氟雷拉纳:国内农药登记空白的第一种异噁唑啉类杀虫剂
有害生物耐药性的发生、发展和高风险农药的禁限用迫切需要新型绿色农药。作为首个商业化的异噁唑啉类杀虫剂,氟雷拉纳已被广泛用于宠物和家禽体外寄生虫防控。随着生产成本的不断降低和研究应用的逐渐深入,氟雷拉纳作为农药进行开发的可能性凸显,具有较好的市场前景。本文对氟雷拉纳的理化性质、毒性、作用机制、生物活性、抗性、代谢残留、合成分析、制剂开发和应用等进行总结介绍,旨在为氟雷拉纳等异噁唑啉类杀虫剂作为农药的研究开发、原药登记与产品应用提供指导。
氟雷拉纳(Fluralaner)是日本日产化学株式会社于2004年首次发现,凭借新颖的作用机理,兼具广谱高效的杀虫活性、优异的环境生态安全性,综合性能突出。氟雷拉纳是第一种异噁唑啉类杀虫剂,在氟苯虫酰胺(鱼尼丁受体调节剂)的衍生化过程中,通过将氟苯虫酰胺中的七氟异丙基替换为杂环结构,同时保留双酰胺骨架,可以开发出含有异噁唑啉环的杀虫剂分子;随后,通过对酰胺键构型进行反转修饰,成功合成氟雷拉纳。后续研发的异噁唑啉类杀虫剂均以氟雷拉纳为先导化合物衍生而来。氟雷拉纳首先被美国FDA批准(商品名:Bravector)上市,对于猫、狗的体外寄生虫有较好的防治作用,该产品于 2020 年在中国获批作为兽药上市,目前其作为兽药已实现产业化,国内化工企业对其中间体供应、合成工艺优化的技术储备充足。另有行业传言称,氟雷拉纳若作为农药活性成分使用,对蓟马具有优异的防治效果;不过截至目前,该化合物尚未在美国、欧盟、中国等主要国家和地区完成农药登记。氟雷拉纳作为一款兼具杀虫、杀螨活性且市场潜力巨大的化合物,其农药登记的商业价值突出,建议对该产品农药登记布局感兴趣的企业持续重点关注,以抢抓市场布局的先机。
一、前言
作为农业生产资料,农药在保护农林园艺作物、保障粮食安全和促进公共环境、卫生健康等方面具有重要的作用。然而,随着传统农药品种的反复使用,气候环境和作物种植结构的变化,有害生物对现有农药品种的耐药性不断增强。加上高风险农药禁限用的范围扩大,新型绿色农药的研究开发和应用显得更为迫切。
异噁唑啉类杀虫剂(含杀螨剂)以其全新的化学结构、独特的作用机制、广谱高效的生物活性以及良好的哺乳动物安全性,逐渐成为继新烟碱、芳基吡唑、大环内酯和双酰胺杀虫剂后的又一重要品类。异噁唑啉类杀虫剂的研发源于植保杀虫剂的创制,但早期却因为生产成本等因素的限制,主要被用于宠物和家禽的体外寄生虫防控。后来,随着研究的不断深入,以氟噁唑酰胺和异噁唑虫酰胺为代表的异噁唑啉类杀虫剂在农业上的开发应用取得了成功,逐渐成为有害生物综合治理和抗性防治的重要工具。图 1 列述了 12 个具有商业化价值的异噁唑啉类杀虫剂新品种,可分为苯甲酰胺(深蓝色)、萘甲酰胺(天蓝色)、螺环胺(绿色)和噻吩甲酰胺(紫色) 4 个二级类别(图 1)。其中,苯甲酰胺二级类别已成为农药创制和开发的热点。
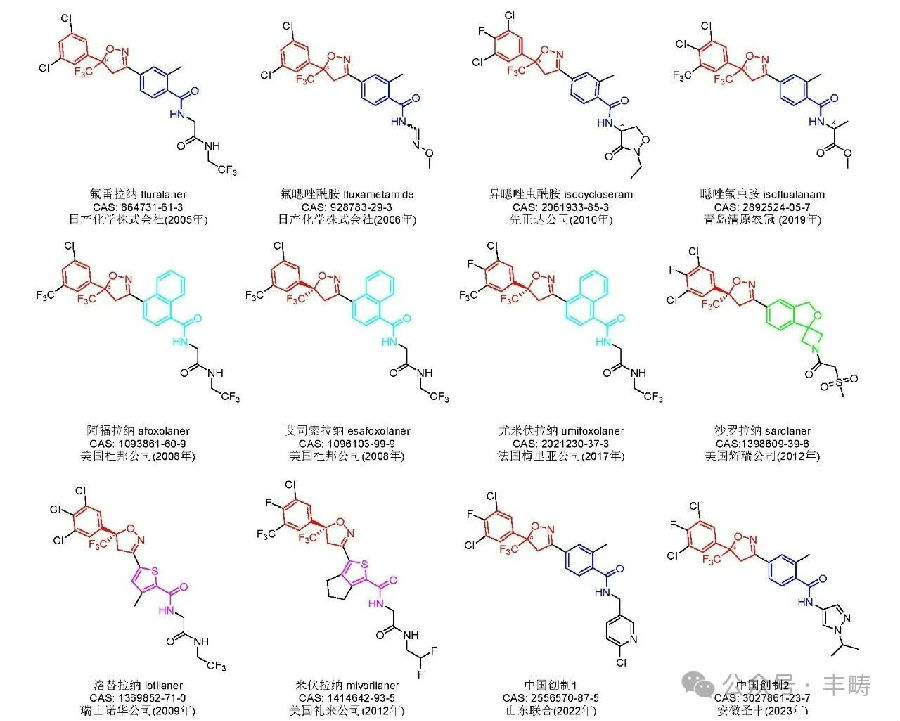
图 1 氟雷拉纳及其他具有商业化价值的异噁唑啉类杀虫剂
作为苯甲酰胺二级类别中的重要代表,氟雷拉纳是首个商业化的异噁唑啉类杀虫剂,由日本日产化 学 株 式 会 社 创 制 报 道, 代 号 A?1443 和 AH252723。得益于氟雷拉纳优异的蜱螨蚤虱杀灭活性和哺乳动物安全性,美国默克公司最早将其作为宠物杀外寄生虫剂进行开发,商品名 Bravecto®(13.64%氟雷拉纳咀嚼片),后又以商品名一锭除®(外用滴剂)和贝卫多®(氟雷拉纳咀嚼片和滴剂)在中国台湾和大陆上市。目前,氟雷拉纳已成为动物保护领域销售额最大的产品。
随着氟雷拉纳等异噁唑啉类杀虫剂在生产成本上的突破,以及在顽固性和抗药性害虫防治研究上的深入,氟雷拉纳等作为农药进行开发的可行性在不断增强。目前,还鲜见氟雷拉纳作为农药研究和应用的系统报道。本文从理化性质、毒性、作用机制、生物活性、抗性、代谢残留、合成分析、制剂开发和应用等方面对氟雷拉纳的研究进展进行总结,以期为氟雷拉纳等异噁唑啉类杀虫剂作为农药的研究和应用提供参考。
二、理化性质
氟 雷 拉 纳 的 IUPAC 化 学 名 称 为 4?[(5RS)?5?(3,5?二氯苯基)?5?三氟甲基?4,5?二氢异噁唑?3?基]?2?甲基?N?{2?氧代?2?[(2,2,2?三氟乙基)氨基]乙基}苯甲酰胺,分子式 C22H17Cl2F6N3O3, 分子量556.29。
氟雷拉纳原药为类白色至白色粉末,无臭味,熔点 173.3~175.5 °C,闪点 236 °C,蒸气压 < 1.0 ×10?5Pa(20 °C),正辛醇/水分配系数 LogPow4.5,有机碳吸附系数 LogKoc为 4.1,生物浓缩系数 BCF 为 79.4 L/kg(斑马鱼),好氧土壤 DT50典型值为 60 d,具有低生物富集性和中度持久性。氟雷拉纳在水中稳定,最小点火能为 30~100 mJ,燃烧数为 2 (25 °C),粉尘爆燃指数 Kst为 170 m·bar/s,属于不易燃易爆物质,也不具有氧化性,但应避免与氧化物质接触或混合。氟雷拉纳可溶于甲苯、丙酮、乙腈和甲醇而微溶于正己烷,水中溶解度 0.082 mg/L,与氟噁唑酰胺和异噁唑虫酰胺相比,氟雷拉纳的水溶解度居中、蒸气压高而 LogPow值最小。
氟雷拉纳为外消旋体,包括(S)?氟雷拉纳(开发代码 A664)和(R)?氟雷拉纳(开发代码 A663)。(S)?氟雷拉纳(e.e.>99%)熔点为 173.0~175.0 °C,[α]23.1D为+61.96 (C=1.10,乙醇);(R)?氟雷拉纳(e.e.>99%)为非晶态,[α]23.1D为?58.95 (C=1.15,乙醇)。
三、毒性
——哺乳动物毒性
氟 雷 拉 纳 对 哺 乳 动 物 低 毒 : 大 鼠 的 经 口LD50>2000 mg/kg、经皮 LD50>2000 mg/kg;兔子皮肤无刺激性,豚鼠无致敏性,但兔子眼睛有中等刺激性。氟雷拉纳无基因毒性:鼠伤寒沙门氏菌回复突变(Ames)、小鼠淋巴瘤和染色体畸试验,以及小鼠骨髓微核试验结果均呈阴性。氟雷拉纳可能会对未出生的婴儿造成影响:大鼠 1 代和 2 代经口生 育 毒 性 的 无 明 显 损 害 作 用 水 平 (NOAEL) 分 别为 75、50 mg/kg,大鼠经口发育毒性的 NOAEL 为100 mg/kg,兔子经口和经皮发育毒性的 NOAEL 分别为 10、100 mg/kg 。日本食品安全委员会制定的每日允许摄入量(ADI)为 0.01 mg/kg。
氟雷拉纳对脊椎动物的神经系统存在一定的药理副作用。在给药约 24 h 后,科克尔犬出现短暂性的全身性共济失调、肌阵挛性抽搐、头部和身体震颤、肌肉抽搐和口腔吞咽困难等神经毒性症状。但该症状无需任何处理即可在 10 h 后自动完全康复。
——生态毒性
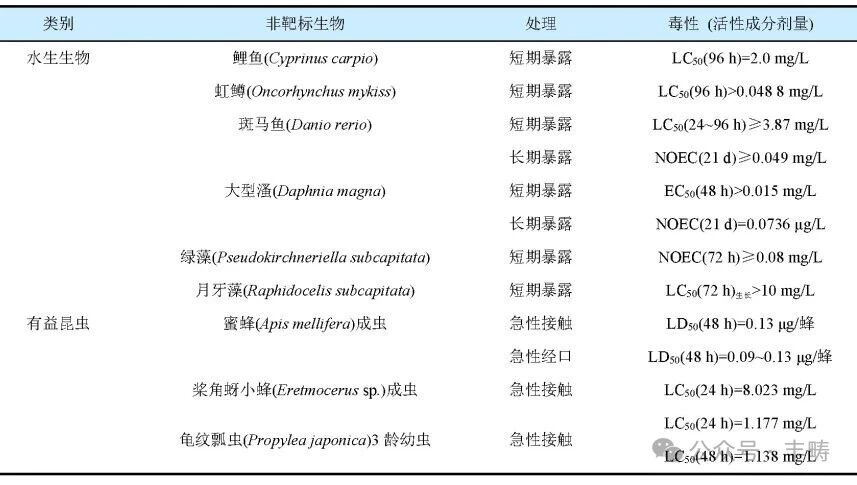
由表 1 可知,氟雷拉纳对水生生物和有益节肢动物的毒性较高,其中对鱼和藻类植物具有中等毒性,对大型溞和蜜蜂高毒。然而,氟雷拉纳及其兽用制剂对斑马鱼的毒性较低,可在斑马鱼体内迅速浓缩,并在清水中暴露后消除:氟雷拉纳 2.00、0.20 mg/L 培养液的 BCF 分别为 12.06 (48 h)和 21.34(144 h);暴露 15 d 后再在清水中进行消除处理 6 d,斑马鱼体内的氟雷拉纳浓度仅为 0.113 mg/kg。由于氟雷拉纳具有高疏水性,能够穿透、保持和积聚在脂质膜上至有毒的局部浓度,并进入与受体结合,长时间暴露或其他不当处理可能会使氟雷拉纳在不同的膜和器官中达到高浓度而对脊椎动物造成危险。
表 1 氟雷拉纳的生态毒性
四、作用机制
——作用方式
作为兽药,氟雷拉纳属于具有全身作用的杀寄生虫剂,对动物表皮具有较好的渗透性。作为农药,尚不清楚其在植物体内是否具有内吸传导和跨层转移活性。根据生物活性测试结果推断,氟雷拉纳应以胃毒作用为主,兼具一定的触杀作用。以外引红火蚁(Solenopsis invicta)为例,氟雷拉纳一般通过个体接触和喂食在工蚁之间传播而使其巢穴同伴产生毒性反应。
——生物化学
(1)作用靶标与作用力
与其他异噁唑啉类杀虫剂相同,氟雷拉纳为多作用靶标杀虫剂,主要靶向γ?氨基丁酸门控氯离 子 通 道 (GABA?Cl) 和 谷 氨 酸 门 控 氯 离 子 通 道(Glu?Cl)等配体门控氯离子通道受体。对家蝇、草地贪夜蛾、埃及伊蚊(Aedes aegypti) 和桔小实蝇(Bactrocera dorsalis)的电生理学试验结果确认,氟雷拉纳对γ?氨基丁酸(GABA)诱导的氯离子流具有较强的抑制作用。同时,氟雷拉纳还可阻滞谷氨酸(Glu)诱导的氯离子流,且该阻滞作用仅约为 GABA诱导的 1/52~1/15。
穿透靶标受体亚基界面后,氟雷拉纳与受体亚基 关 键 氨 基 酸 残 基 通 过 氢 键 等 相 互 作 用 而 对GABA?Cl 受体和 Glu?Cl 受体发挥作用。对放射性配体[3H]EBOB 与家蝇受体结合的抑制作用以及对家蝇 Glu 诱导氯离子流的阻滞作用:(S)?氟雷拉纳>氟雷拉纳>氟虫腈> (R)?氟雷拉纳;而对家蝇GABA 诱导氯离子流的阻滞作用:氟雷拉纳> (S)?氟雷拉纳>氟虫腈> (R)?氟雷拉纳。其中,(S)?氟雷拉纳对家蝇[3H]EBOB 结合、GABA?Cl 受体和Glu?Cl 受体的抑制作用分别约是(R)?氟雷拉纳的1234、1009、250 倍,这说明 GABA?Cl 受体是氟雷拉纳的主要作用靶标,而(S)?对映体为氟雷拉纳的主要作用成分。
推测氟雷拉纳的作用机制与氟噁唑酰胺、异噁唑虫酰胺、溴虫氟苯双酰胺(brofanilide)和环丙氟虫胺(cyproflanilide)类同,主要为 GABA?Cl 受体变构调节剂,与氟虫腈等 GABA?Cl 拮抗剂和阿维菌素等 Glu?Cl 调节剂不同。虽然氟雷拉纳对敏感性靶标受体的作用力不敌氟虫腈和阿维菌素等传统杀虫剂,但对抗性靶标受体的作用力却出现反超。对于GABA?Cl 敏感受体,氟雷拉纳对 GABA 诱导电流的抑制作用不敌阿维菌素和氟虫腈;对于抗狄氏剂(RDL)亚基同聚的 GABA?Cl 受体,氟雷拉纳的作用效力比苦味宁(picrotoxinin)和狄氏剂(dieldrin)高出几个数量级,比氟虫腈高 5~236 倍;对于敏感性 Glu?Cl 受体,氟雷拉纳对 Glu 诱导电流的抑制作用比氟虫腈低而比阿福拉纳高。
此外,氟雷拉纳与 GABA?Cl 和 Glu?Cl 受体的结合可被阿维菌素有效地抑制,这与氟虫腈和硫丹等杀虫剂不同。
氟雷拉纳在激活构象状态比静息构象状态 对GABA?Cl 受体的拮抗作用更为明显,这说明氟雷拉纳可能通过与 GABA?Cl 受体激活构象逐步融合到达结合位点并与之结合来发挥作用。双电极电压钳(TEVC)电生理学研究结果表明,在 GABA?Cl受体静息状态时,氟雷拉纳不影响 GABA 的响应;在氟雷拉纳存在时,持续快速添加 GABA 可促使氟雷拉纳的抑制作用达到稳态;而一旦受到抑制,GABA 的响应将是不可逆的。
(2)GABA?Cl 作用靶标
氟雷拉纳对主要作用靶标 GABA?Cl 受体的作用位点等与氟虫腈、狄氏剂、硫丹和林丹等传统杀虫剂存在差异。RDL 亚基第二跨膜区域(TM2,其余 3 个跨膜区域为 TM1、TM3 和 TM4)的丙氨酸(A2′TM2)突变是靶标节肢动物对狄氏剂(A2′STM2)和氟虫腈(A2′NTM2)产生靶标抗性的关键因素,但该位点 突 变 对 氟 雷 拉 纳 的 敏 感 性 无 影 响。 对 于GABA?Cl 受体亚基中的 A301HTM2/T350ATM3双位点基因突变后的二斑叶螨和 A283N 单位点基因突变后的灰飞虱(Laodelphax striatellus),氟虫腈对 GABA诱导其氯离子电流的抑制作用和生物活性显著降低,而氟雷拉纳则对其无影响。
一般认为氟雷拉纳对 GABA?Cl 受体的作用位点位于亚基之间的 TM1~TM3 跨膜区域表面。对家蝇定点突变 RDL 同聚体的 TEVC 电生理学研究结果表明,TM1~TM3 中的多个氨基酸残基在氟雷拉纳的拮抗作用中起关键作用。其中,GABA?Cl受体亚基 TM1 中的点突变 G271L、L278C 和 I274C,TM3 中的点突变 G333和 F336(根据 Glu?Cl 受体等 效 推 测 ), 以 及 TM2 中 的 点 突 变 M312S 和N316L都会导致氟雷拉纳的敏感性显著降低,但 TM1 中的点突变 I274A 和 I274F以及 TM2 中的点突变 S313A 和 S314A则对氟雷拉纳的敏感性没有影响。虽然点突变 N316L 因涉及 2 个密码子核苷酸改变而不容易发生,但该突变对溴虫氟苯双酰胺和氟虫腈的敏感性却无影响,显示出了氟雷拉纳与溴虫氟苯双酰胺和氟虫腈的差异。
进一步的研究表明,纯合 G3'MTM3 是氟雷拉纳对靶标节肢动物的最重要靶标位点。对水稻二化螟(Chilo suppressalis)潜在氨基酸结合残基(TM1 中的点突变 I258T 和 L275I;TM2 中的点突变 V288I、M298N、G303N 和 A304S;TM3 中的点突变 G3'M/S、A327S、G336N、M338I 和 A339F;TM4 中的点突变 M473V 和 I477D)定点诱变和 TEVC 技术验证结果表明,G3'M 单位点突变的 RDL 同聚 GABA?Cl受体对氟雷拉纳敏感性的抑制能力最强,几乎完全破坏氟雷拉纳和阿维菌素与受体的结合,但对氟虫腈与受体的结合则无影响。对于家蝇幼虫,携带 G3'MTM3的杂合系受体对阿维菌素、氟虫腈、溴虫氟苯双酰胺和 氟 雷 拉 纳 都 没 有 表 现 出 明 显 的 抗 性 ; 而 携 带G3'MTM3 的纯合系受体对氟雷拉纳和溴虫氟苯双酰胺具有高抗性,但对氟虫腈和阿维菌素仍然敏感。
(3)Glu?Cl 作用靶标
对于 Glu?Cl 受体,TM3 中的 L315 的芳香族氨基酸取代点突变可显著提高氟雷拉纳的效力(脂肪族氨基酸取代则不能),同时消除阿维菌素等大环内酯类杀虫剂对 Glu?Cl 的激活作用及对低浓度 Glu 诱导电流的增强作用,但其对高浓度 Glu 诱导电流的拮抗作用则无影响。此外,I253A 单点突变可使氟雷拉纳的效力降低约 2 倍,但使阿维菌素效力提高约 5 倍;M257L、L315F 单点突变和 M257L/T316V双点突变使氟雷拉纳的效力分别提高 4、138、2 倍,但 T316V 单点突变对氟雷拉纳、M257L/T316V 双点突变对阿维菌素的效力均无明显影响。特别地,L315F 单点突变的 Glu?Cl 受体对氟雷拉纳的敏感性比 GABA?Cl 受体对 GABA 的敏感性要高约 6 倍。
(4)亚(半)致死作用
氟雷拉纳的亚(半)致死作用体现为对靶标节肢动 物 的 生 长 发 育 、 存 活 和 繁 殖 等 产 生 影 响 。 经LC10~LC30亚致死浓度的氟雷拉纳处理后,二斑叶螨和柑橘红蜘蛛雌性成虫的寿命、繁殖力和净生殖率(R0)均缩短或降低,但生命周期(T)都无变化,二斑叶螨的内禀增长率(r)和有限增长率(λ)在 LC30处 理 时 显 著 降 低 而 在 LC10处 理 时 无 显 著 变 化。LC30亚致死浓度和 LC50半致死浓度的氟雷拉纳都可抑制多种果蝇的繁殖力和存活率,LC50处理会刺激桔小实蝇的繁殖力和南亚果实蝇(Bactrocera tau)的存活率,同时影响瓜实蝇(B. cucurbitae)和南亚果实蝇后代的孵化率并降低雌性后代的比例而呈现出明显的跨代效应。较高亚致死浓度的氟雷拉纳(20、25、45 μg/L)对埃及伊蚊、斯氏按蚊和致倦库蚊的繁殖力、卵孵化成功率等生活史特征产生显著的负面影响。可能与其他杀虫剂相似,氟雷拉纳通过干扰靶标节肢动物的生理过程和行为来实现其亚(半)致死作用。如 0.022%、0.045%氟雷拉纳的肉糜和水凝胶饵料显著减少了美国西部胡黄蜂(Vespulapensylvanica)的觅食。
在生长发育方面,氟雷拉纳对斜纹夜蛾的亚致死效应包括幼虫体重减轻、化蛹和羽化减少、成虫羽翼呈切痕,并伴有对昆虫发育重要基因几丁质酶 5(CHT5)和保幼激素酸性甲基转移酶(JHAMT)转录水平的变化。这可能与氟雷拉纳处理使斜纹夜蛾相关基因表达上调或下调有关。LC30和 LC50处理斜纹夜蛾的差异表达基因(DEG)分别为 3275、2491 个,至少 16 个细胞色素 P450 酶(CYP 或 P450)、1 个谷胱甘肽S?转移酶(GST)和 3 个羧酸酯酶(CarE)与解毒作用相关,1 个几丁质和 4 个幼激素合成基因与生长相关。其中,编码多个 CYP、GST、热休克蛋 白 68(HSP 68) 、 液 泡 蛋 白 分 选 相 关 蛋 白 13(VPSAP13)、钠偶联单羧酸转运蛋白 1(SCMT1)、蛹表皮蛋白(PCP)、蛋白外带(PT)和低密度脂蛋白受体转换蛋白 1?b(LDLRAP1?B)的基因相对表达量显著上调;酯酶、硫转移酶 1C4、质子偶联叶酸转运蛋白、几丁质酶 10、125 kDa 凝胶相关蛋白(GRP)、丝素重链(FHC)、脂肪酸合成酶和一些 CYP 的编码基因显著下调。
氟雷拉纳对有益节肢动物的亚(半)致死作用效果与氟雷拉纳浓度和昆虫种群类别等有关。虽然LC15和 LC50的 氟 雷 拉 纳 都 可 使 蒙 氏 桨 角 蚜 小 蜂(Eretmocerus sp.)的寿命显著缩短,其选择安全性不敌双丙环虫酯和嗪虫唑酰胺,且 LC50使雌成虫的寄生率及其后代羽化率分别显著上升和降低,LC15处理则对后代发育历期无显著影响。然而,对于龟纹瓢虫,LC10和 LC30的氟雷拉纳对其体重、发育时间、产卵前期和繁殖力等生活史特征都无显著不利影响。
暴露于亚致死浓度的氟雷拉纳(2.00 mg/L)后,斑马鱼体内的过氧化氢酶(CAT)和 CarE 活性受到显著调节,超氧化物歧化酶(SOD)、GST、谷胱甘肽过氧化物酶(GSH?Px)酶活性及脂质过氧化物丙二醛(MDA)含量保持稳定水平;CYP1C2、CYP1D1、CYP11A 的转录表达在暴露 12 h 时显著下调。这说明,抗氧化防御和代谢系统参与氟雷拉纳诱导的毒性,CAT 和 CarE 活性及大部分 CYP mRNA 表达水平对氟雷拉纳亚致死浓度有快速响应。
(5)选择安全性
氟雷拉纳对哺乳动物相对安全,对家蝇等靶标有害节肢动物具有较高的选择毒性。一方面,氟雷拉纳对哺乳动物和昆虫体内受体的亲和力存在差异;另一方面,哺乳动物和昆虫在细胞膜组成上的差异可能会非特异性地影响作用于 GABA?Cl 受体杀虫剂的选择性,调节氟雷拉纳的溶解度及其对GABA?Cl 受体的靠近。放射性配体结合和荧光膜电位染色试验结果表明,氟雷拉纳对大鼠和猫体内受体的作用力约为家蝇和黑腹果蝇的 10 000 倍以上。对于 GABA?Cl 受体,氟雷拉纳对昆虫的亲和力大于哺乳动物的,对人的 GABA?Cl 受体几乎无作用,对大鼠的脑膜蛋白结合作用低[40]。有趣的是,小鼠β2 同源五聚体 TM3 中的 M3'G 位点突变会提高重组异聚 Mmα1β2?M3'G 通道对氟雷拉纳的敏感性。
此外,同源性建模和分子对接结果表明,(S)?氟雷拉纳对 GABA?Cl 受体具有更好的结合亲和力,而大鼠肝微粒体对(R)?氟雷拉纳具有一定的立体选择性代谢,即(R)?氟雷拉纳更容易被哺乳动物代谢而安全性更高。与其他异噁唑啉类杀虫剂相比,氟雷拉纳对哺乳动物的选择安全性要略低。对人和犬的 GABA?Cl 受体研究结果表明,氟雷拉纳的半抑制浓度(IC50)为 1.9~13 μM,低于沙罗拉纳、阿福拉纳和洛替拉纳。
五、生物活性
——杀虫/螨活性
与氟噁唑酰胺和异噁唑虫酰胺等异噁唑啉类杀虫剂类同,氟雷拉纳对鳞翅目、缨翅目、双翅目、鞘翅目、同翅目、蜚蠊目、半翅目、蜱螨目和蚤目等多类别有害节肢动物具有广谱杀灭活性。室内试验结果表明,氟雷拉纳 100~500 mg/L 对不同发育阶段的多种有害节肢动物均具有 80%以上杀灭活性(表 2)。
表 2 氟雷拉纳的杀虫/螨活性
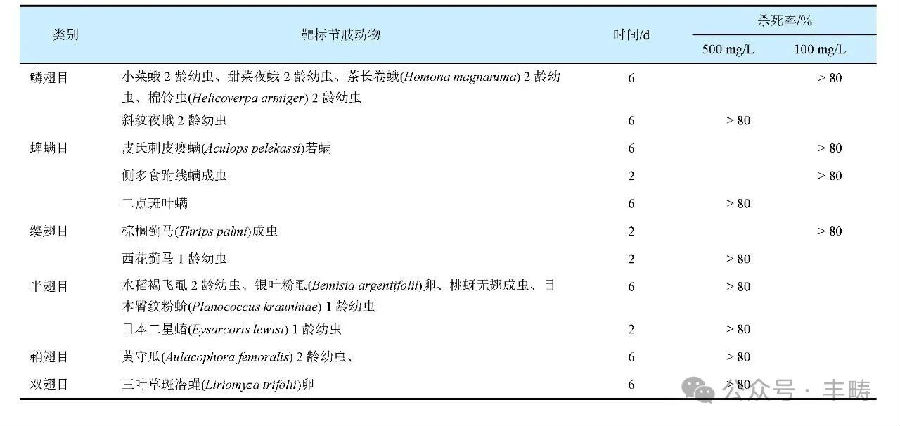
与氟噁唑酰胺相同,(S)?氟雷拉纳的生物活性明显优于(R)?氟雷拉纳(表 3)。其中,(S)?氟雷拉纳对农业害虫二化螟和灰飞虱的杀虫活性约为(R)?氟雷拉纳的 33.8~39.0 倍,(R)/(S)活性比略低于其对动物蜱螨目害虫的(约 1/10 000~1/625)。
表3 氟雷拉纳及其对映体的生物活性比较
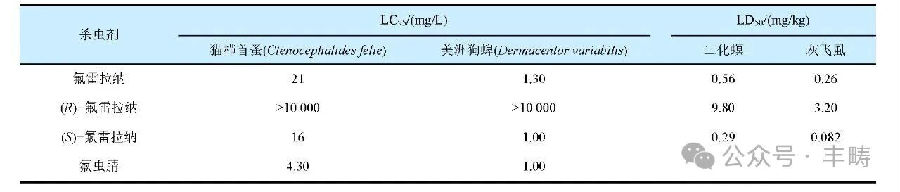
进一步的研究结果(表 4)表明,不同处理方式的氟雷拉纳对农业和公共卫生领域的多种有害节肢动物也具有较高生物活性,多优于氟噁唑酰胺、阿福拉纳、洛替拉纳、氟虫腈、毒死蜱、溴氰菊酯、四氯虫酰胺和呋虫胺等杀虫剂,而与甲氨基阿维菌素苯甲酸盐和阿维菌素等杀虫剂大致相当。同时,氟雷拉纳对小菜蛾、草地贪夜蛾、甜菜夜蛾、玉米黏虫、茄二十八星瓢虫、普通大蓟马、黄曲跳甲、二斑叶螨、朱砂叶螨、台湾乳白蚁和果实蝇的活性突出;对于蚊虫,氟雷拉纳的击倒作用和毒力优于其他异噁唑啉类杀虫剂而持效期优于阿维菌素;对于水稻灰飞虱等害虫,虽然氟雷拉纳对敏感性种群的生物活性不敌氟虫腈,但对抗性种群的生物活性却远胜于氟虫腈。
表4 不同处理方式的氟雷拉纳对有害节肢动物的生物活性
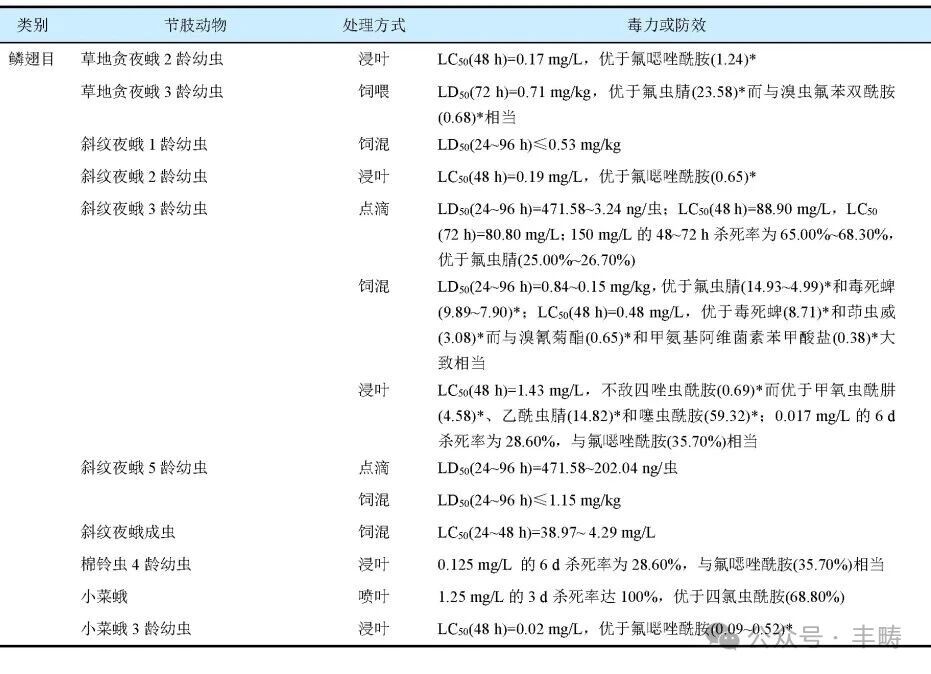

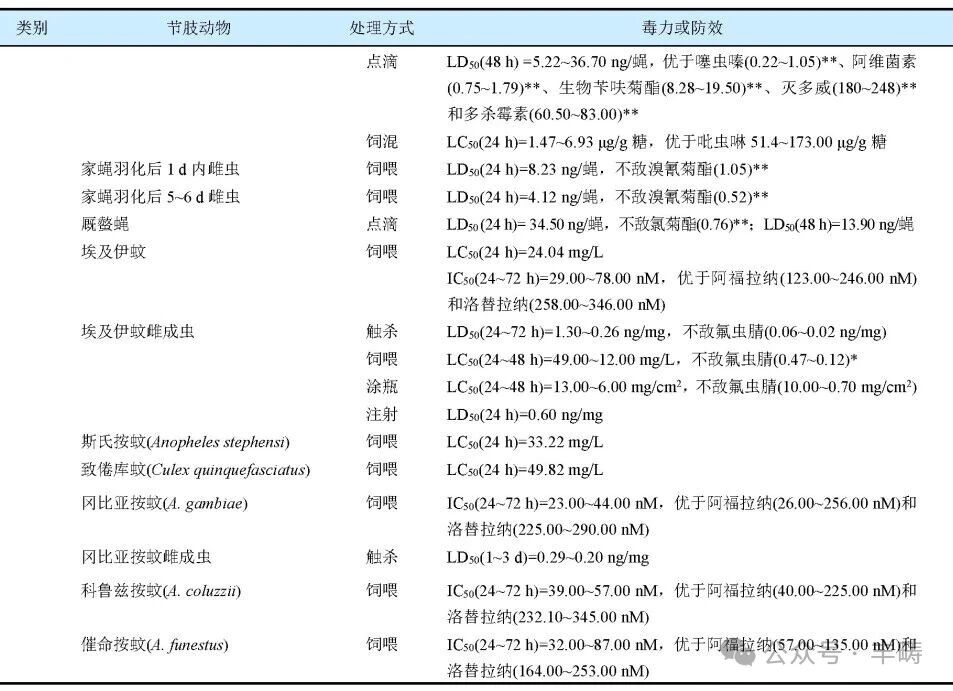
注:*代表前括号内数值单位mg/L;**代表前括号内数值单位ng/蝇
对于同种有害节肢动物,氟雷拉纳对低龄幼虫的活性优于高龄幼虫,胃毒作用优于触杀作用,浸叶处理优于点滴处理。而对于外引红火蚁,工蚁对氟雷拉纳的敏感性高于 4 龄幼虫。非靶向代谢组学研究结果表明,在氟雷拉纳 10 mg/L 暴露胁迫下,幼蚁和工蚁的差异代谢产物主要集中在有机酸及其衍生物、脂类和类脂分子、核苷、核苷酸及其类似物,差异代谢反应主要在能量代谢、解毒代谢和神经递质配体。当受到氟雷拉纳胁迫时,工蚁消耗更多精氨酸合成途径底物(L?谷氨酸、L?天冬氨酸和富马酸)来为农药的解毒(谷胱甘肽)提供能量,而L?天冬氨酸的高积累引起了工蚁的兴奋性毒性;幼蚁消耗更多的花生四烯酸来合成前列腺素 D2 (PG D2),同时儿茶素、橙皮苷和L?抗坏血酸等抗氧化剂代谢的变化表明,幼蚁比工蚁更有能力清除活性氧(ROS)反应。
——其他活性
氟雷拉纳可通过抑制细菌增殖,抑制或清除生物被膜的形成等机制对病原菌产生一定抗菌作用,具有不易产生耐药突变等优点。研究表明,氟雷拉纳对革兰氏阳性致病菌金黄色葡萄球菌(Staphylococcusaureus)的最低抑菌浓度(MIC)和最低杀菌浓度分别为 4~8、8~16 mg/L,且与阿米卡星(amikacin)混用具有协同抗菌活性。由此推测氟雷拉纳对农业植物病原菌(特别是细菌性病原菌)可能存在一定的生物活性,值得关注和研究。
六、抗性
当前,氟雷拉纳主要作为动物保健产品使用,有关其对农业和公共卫生有害节肢动物抗药性的监测和研究报道相对较少。2017—2020 年对江苏 3 地的田间害虫抗性监测结果表明,二化螟种群已对氯虫苯甲酰胺、阿维菌素和杀虫单等杀虫剂产生了不同程度的抗性,但对氟雷拉纳还处于敏感水平。
——交互抗性
根据国际杀虫剂行动委员会对杀虫剂的分组以及氟雷拉纳的作用机制,推测氟雷拉纳与溴虫氟苯双酰胺等间二酰胺类杀虫剂和氟噁唑酰胺等其他异噁唑啉类杀虫剂可能存在交互抗性,但与其他杀虫剂的交互抗性风险相对较小。研究结果表明,氟雷拉纳与氟虫腈对灰飞虱不存在交互抗性,与拟除虫菊酯类杀虫剂对黑腹果蝇不存在交互抗性,但与氯菊酯对家蝇存在轻微的点滴处理交互抗性,而与吡虫啉对家蝇饲喂处理不存在交互抗性。
——抗性机制
与鱼尼丁靶标杀虫剂和弦音器 TRPV 通道靶标杀虫剂等类同,靶标节肢动物对氟雷拉纳产生抗性的机制主要可能涉及解毒酶和转运蛋白表达上调、复制和突变介导的代谢抗性、靶标受体基因突变和表达变化介导的靶标抗性以及穿透抗性降低等因素。
对外引红火蚁生化变化探究的结果表明,P450 和 CarE 可能参与氟雷拉纳的解毒,而 GST 则没有。对草地贪夜蛾的研究结果则表明,P450 和GST 对氟雷拉纳的摄入具有显著的正响应,而 CarE则没有。在进一步的增效试验中,P450 抑制剂增效醚(PBO)可增加氟雷拉纳对外引红火蚁和斜纹夜蛾的毒性并抑制家蝇对氟雷拉纳的抗性,RNAi处 理 抑 制 P450 基 因 CYP9AS16 、 CYP6AS161 、CYP6SQ20 和 CYP336A45 表达可提高外引红火蚁对氟雷拉纳的敏感性。由于氟雷拉纳抗性作为不完全显性性状的中间遗传,解毒酶 P450 对介导氟雷拉纳的抗性起重要作用。
二化螟、黑腹果蝇、蜜蜂和灰飞虱的 GABA?Cl受体亚基 TM3 中的 G3'位点突变导致昆虫对氟雷拉纳敏感性显著下降。在使用 dsRNA 抑制埃及伊蚊RDL mRNA 的表达后,暴露于氟雷拉纳的埃及伊蚊幼虫和成年雌蚊的死亡率显著降低,说明 RDL 基因表达减少导致昆虫对氟雷拉纳的敏感性降低。
表皮穿透性降低也被证明是家蝇对氟雷拉纳产生抗性的又一重要机制,抗性系数可高达 10 000 倍。氟雷拉纳与噻虫嗪、生物苄呋菊酯、阿维菌素、灭多威和多杀霉素点滴处理家蝇可产生比残留暴露和饲喂处理更高的交互抗性水平,但与分子量、代谢不稳定性、蒸气压和LogP等因素无关。
为适应对氟雷拉纳的抗性,靶标节肢动物在适合度代价方面进行了权衡。黑腹果蝇的 GABA?Cl受体亚基 TM3 中的 G3'M 突变可使其卵正常孵化得到对氟雷拉纳有高抗性的初孵幼虫,但后者的运动能力下降并在蛹期前死亡。RDL 亚基中 N316L 点突变后的家蝇对氟雷拉纳产生抗性的同时还会因卵巢畸变和卵子发育不良而导致雌虫不育。
七、代谢残留
氟雷拉纳在哺乳动物体内的代谢产物以母体化合物为主,其余还有苯甲酰胺支链酶解产物4?[(5RS)?5?(3,5?二氯苯基)?5?三氟甲基?4,5?二氢异 唑?3?基]?2?甲基苯甲酰胺(1)及其进一步水解产物 4?[(5RS)?5?(3,5?二氯苯基)?5?三氟甲基?4,5?二氢异 唑?3?基]?2?甲基苯甲酸(2)。代谢物1和2的化学结构见图 2。此外,氟雷拉纳单羟化、双羟化产物及其进一步磺化产物也占有一定比例,但这些代谢物的化学结构还有待进一步研究确认。
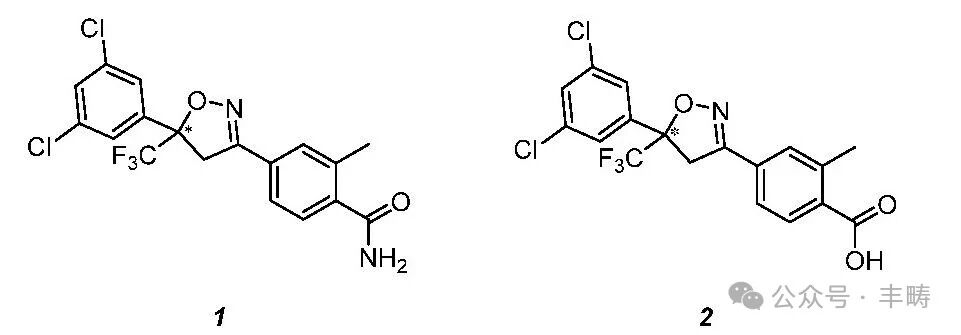
图 2 氟雷拉纳的 2 个代谢产物的化学结构
在欧盟,氟雷拉纳在鸡可食性组织及鸡蛋中的最大残留限量(MRL,单位:μg/kg)规定如下:肌肉 65,皮肤和脂肪、肝脏 650,肾脏 420,鸡蛋 1300。作为进口兽药成分,中国农业农村部暂时也对这一规定采纳试行。然而,作为农药,氟雷拉纳在作物上的 MRL 和相关残留分析方法还未见报道。
八、合成与分析
——原药合成
(1)氟雷拉纳的合成
氟雷拉纳可基于中间体 4?溴?3?甲基苯甲醛(3)、2?甲基?4?甲酰基苯甲酸(4)、3?甲基苯乙酮(5)、2?甲基?4?乙酰基苯乙腈(6)、4?溴?2?甲基苯甲酸(7)和2?甲基?4?乙酰基苯甲酸(8) 为起始原料,采用不同的策略和路线进行合成(图 3)。成环可采用 1,3?偶极加成、分子内亲核加成和氧化加成 3 种不同的策略,一般认为后 2 种优于前 1 种,且先环合优于后环合。在实际生产过程中,应关注对原药中杂质、晶型和对映体的确认和控制。
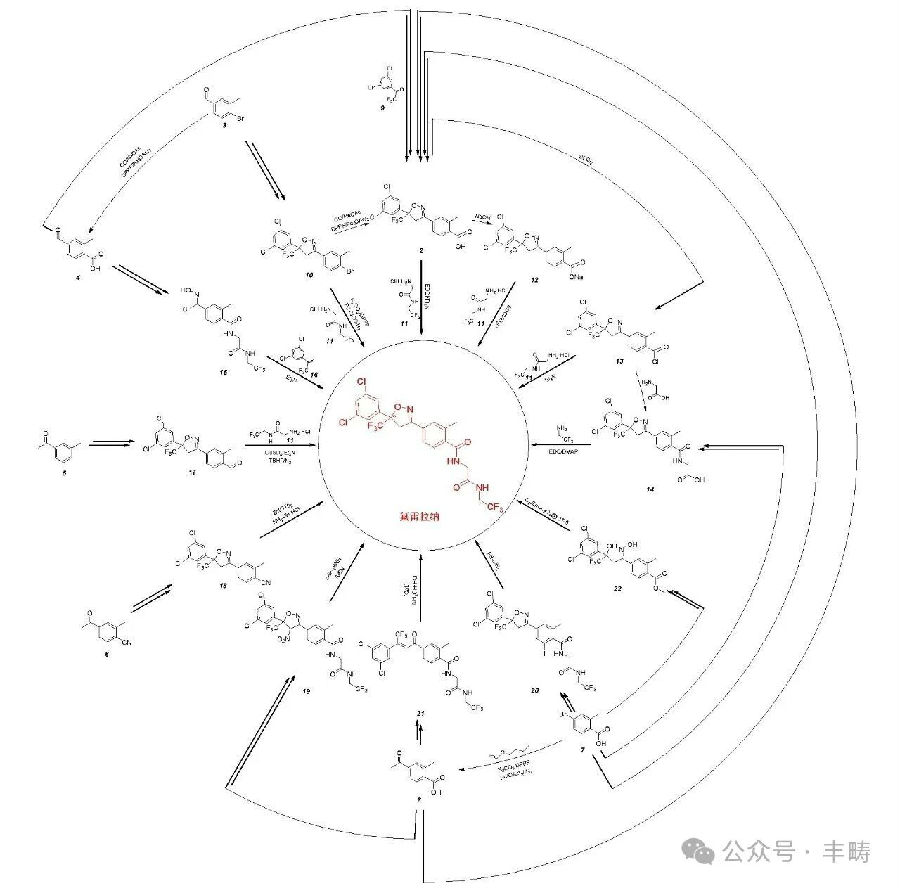
注:图中双箭头表示多步反应(相关反应物和条件未列出),合成路线可能存在多种的仅列出1种。
图 3 氟雷拉纳的不同合成路线
在这些合成路线中,氟雷拉纳可共用其他异噁唑啉类杀虫剂的中间体,如阿福拉纳、艾司索拉纳、尤米伏拉纳和洛替拉纳的中间体 2?氨基?N?(2,2,2?三氟乙基)乙酰胺盐酸盐(11),氟 唑酰胺的中间体3', 5'? 二 氯 ?2, 2, 2? 三 氟 苯 乙 酮 (9) 或 1,3? 二 氯?5?(3,3,3?三氟丙基?1?烯?2?基)苯(16)。特别地,关键中间体(2)既是氟雷拉纳的合成关键中间体和哺乳动物代谢的产物,也是氟噁唑酰胺工业化生产的关键中间体。
(2)(S)?氟雷拉纳的合成
(S)?氟雷拉纳可采用与氟雷拉纳相同的起始原料进行不对称合成,也可直接由氟雷拉纳进行手性分离拆分制备(图 4)。工业上一般采用不对称合成来生成(S)?氟雷拉纳,由烯酮中间体21在手性催化剂的作用下环合得到,或由关键中间体2的(S)?对映体(2S)直接缩合得到。
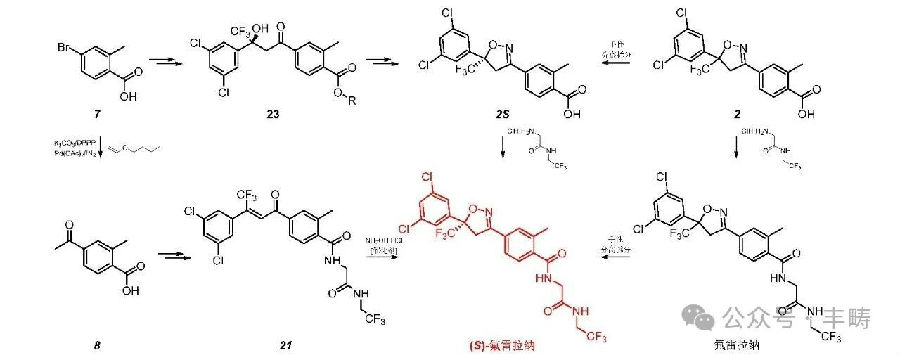
注:图中双箭头表示多步反应(相关反应物和条件未列出),合成路线可能存在多种的仅列出1种。
图 4 (S)?氟雷拉纳的不同合成路线(R=H 或 CH3)
——分析
氟雷拉纳含量可以体积分数为 40%~60%的乙腈/水溶液为流动相,使用 Waters XTerra RP 8 色谱柱(4.6 mm×250 mm,5 μm)的反相高效液相色谱仪在柱温 25~40 °C和波长 245~255 nm 时测定。对于氟雷拉纳的一对对映异构体,可以采用 2 种不同的方法进行测定:① 以体积比为 60∶40 的正己烷/无水乙醇混合溶液为流动相,使用带 CHIRALPAK®AD?H 手性色谱柱(250 mm × 4.6 mm, 5 μm)的高效液相色谱仪在柱温室温和波长 265 nm 时对其进行分离测定;② 直接以直链淀粉?三(3,5?二甲基苯基氨基甲酸酯)键合硅胶为固定相对其进行分离和含量测定。
九、制剂开发与应用
——制剂开发
作为兽药,氟雷拉纳常被制成咀嚼片、滴剂、可溶性粉和溶液等单剂和复方制剂。而作为农药,由于熔点较高且难溶于水而易溶于有机溶剂,氟雷拉纳理论上可制成EC、SL、SC、WP、WG、GR和DP等制剂类型产品。在制剂配方研究和生产时,为减少对氟雷拉纳动物表皮渗透性的影响而影响产品药效,应减少或避免极性碳酸酯、碳酸丙烯酯和柠檬酸三乙酯等溶剂的使用。日本日产化学株式会社在专利里给出了用于农业有害节肢动物防治的氟雷拉纳单剂10%WP、3%EC、15%SC、40%WG、3%GR和2%DP等配方,并指出这些制剂可在兑水稀释50~20 000倍后按有效成分剂量0.005~50 kg/hm2进行施用。
除了单用,氟雷拉纳还可与多种杀虫剂进行预混或桶混施用,但需注意选用具有协同增效作用的有效成分及其合适比例。对水稻灰飞虱的药效试验结果表明:氟雷拉纳与毒死蜱混配具有良好的增效作用,与甲维盐混配的增效作用不显著,与吡虫啉按1∶4混配表现为增效作用,但按2∶3和3∶2混配则表现为拮抗作用。对斜纹夜蛾的药效试验结果表明:氟雷拉纳与毒死蜱混用具有良好的增效作用,与茚虫威混用具有协同增效作用,但与溴氰菊酯或甲维盐混用却表现为拮抗作用。此外,氟雷拉纳与四唑虫酰胺、甲氧虫酰肼、乙酰虫腈和噻虫酰胺按一定比例混用对芋田斜纹夜蛾,与丁氟螨酯或乙唑螨腈按一定比例混用对木薯朱砂叶螨都具有显著的增效作用。温室用氟雷拉纳与桨角蚜小蜂混用控制烟粉虱对有益昆虫的种群数量的影响相对较小,说明该杀虫剂有望用于有害节肢动物综合治理。
——制剂应用
目前暂无氟雷拉纳作为农药的田试研究报道和应用登记批准公告。参考同类氟噁唑酰胺和异噁唑虫酰胺的制剂应用情况,建议将氟雷拉纳推广应用于水果、蔬菜、观赏和经济作物等陆生作物的缨翅目、蜱螨目、鳞翅目、半翅目、直翅目、膜翅目和双翅目等类别有害节肢动物防控。
在公共卫生领域,氟雷拉纳与狄氏剂等传统杀虫剂的交互抗性较低,但其对蚊虫的效力居中、触杀活性较低以及作用缓慢等特点使其不适合作为控制蚊虫成虫和病媒喷雾型卫生杀虫剂。但氟雷拉纳饲喂处理对蚊虫的毒力优于其他异噁唑啉类杀虫剂,添加抗生素混合物或改变糖类诱饵不会影响氟雷拉纳对蚊虫的毒力。
十、总结与展望
作为首个商业化的异噁唑啉类杀虫剂,氟雷拉纳源自农用杀虫剂的创制研究,却作为杀外寄生虫剂先得以开发,逐渐在动物保健领域发挥愈发重要的作用。氟雷拉纳的研究和应用,有力地推动了异噁唑啉类杀虫剂的发展,使其逐渐成为重要的兽药和农药品类。随着生产成本下探和研究深入,氟雷拉纳作为农药的开发和应用的潜力进一步凸显。
作为一种潜在的绿色农药新品种,氟雷拉纳具有独特的化学结构和作用机制,对哺乳动物、鸟类和作物安全,对不同生长发育阶段的多种靶标节肢动物敏感种群和抗性种群都具有较高生物活性,有望成为有害生物综合治理 (IPM)和害虫抗性管理(IRM)的新工具。
氟雷拉纳具有高疏水性、较好的动物表皮渗透性和多作用靶标位点,作用机制与氟虫腈和阿维菌素等传统杀虫剂不同、与溴虫氟苯双酰胺也存在差异。氟雷拉纳对有害节肢动物(特别是小菜蛾、黄曲跳甲、乳白蚁以及抗性灰飞虱等)的生物活性优于氟噁唑酰胺和其他常用杀虫剂,同时还具有潜在的杀菌活性。解毒酶表达上调、基因突变和穿透性减弱等是靶标节肢动物对氟雷拉纳产生抗性的重要原因,目前尚未见农业田间害虫/螨的相关抗性报道。
氟雷拉纳的主要活性成分为其(S)?对映体,2 者都可共用氟噁唑酰胺等异噁唑啉类杀虫剂的关键中间体、采用多种不同的合成路线进行合成,再单独或与具有增效作用的农药成分复配制成 EC、SC、WP 和 WG 等农药剂型产品施用。暂无氟雷拉纳在农业和公共卫生领域的田试研究报道和注册登记批准,建议其用于陆生作物上的顽固性和抗药性有害节肢动物防控。然而,与其他农用异噁唑啉类杀虫剂相同,氟雷拉纳也存在着中度持久性,对多种水生生物、传粉昆虫和有益天敌高毒性等问题。
展望未来,应进一步加强氟雷拉纳及其同类杀虫剂作为农药的研究、开发和应用。一方面,探讨氟雷拉纳对鸟蚕、蚯蚓和生态环境的安全性,建立在不同作物上的残留分析方法和 MRL,开展田间试验研究和登记申请,积极推广其应用。一方面,深入开展原药和制剂的创新性研究和开发,实现晶型、杂质和对映体的有效控制,通过不断的技术升级和工艺优化来提高产品的质量和药效、降低生产成本。另一方面,加强靶标有害节肢动物抗性监测和发展机制研究,与其他农药混用或轮换使用、与其他防治措施相结合,建立与产品相关的作物种植实践规范,最大限度地发挥产品药效并避免对水生生物、有益节肢动物和生态环境的不利影响。与此同时,持续以氟雷拉纳、(S)?氟雷拉纳及其同类杀虫剂为先导和基础进行更深入的创制研究,开发更好的绿色农药原药和制剂,不断实现农业的可持续发展。
游客可直接评论,建议先注册为会员后评论!

以上评论仅代表会员个人观点,不代表中国农药网观点!



